
一.判断化学平衡状态的两种方法
1.用本质特征判断
动态标志:v正=v逆≠0
判断依据:正反应速率与逆反应速率相等,即v正=v逆。

(1)同一种物质:该物质的生成速率等于它的消耗速率。
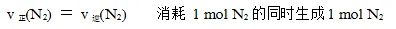
(2)不同的物质:速率之比等于化学方程式中各物质的化学计量数之比,但必须是不同方向的速率。

①在化学方程式两边的不同物质的生成(或消耗)速率之比等化学计量数之比
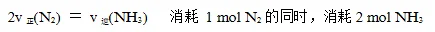
②在化学方程式同一边的不同物质,一种物质的生成速率与另一种物质的消耗速率之比等于化学计量数之比
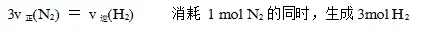
2.用宏观特征判断
(2)静态标志:“变量”不变
判断依据:反应混合物中各组成成分的浓度、含量保持不变。
(1)各组成成分的质量、物质的量、分子数、体积(气体)、物质的量浓度均保持不变。
(2)各组成成分的质量分数、物质的量分数、气体的体积分数均保持不变。
(3)反应物的转化率、产物的产率保持不变。

3.间接标志——“变量不变”
(1)用“总压强、总物质的量、总体积”判断平衡状态的注意事项(PV=nRT)
看气体左右系数和
|
|
|
是否平衡 |
|
压强(恒温恒容) |
当m+n≠p+q时,总压强一定(其他条件一定) |
是 |
|
当m+n=p+q时,总压强一定(其他条件一定) |
不一定 |

(2)气体体积分数/物质的量分数
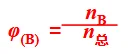

(3)气体平均相对分子质量(m总为气体总质量)
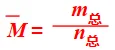
|
|
|
是否平衡 |
|
混合气体的(恒温恒容) |
当m+n≠p+q时,一定 |
是 |
|
当m+n=p+q时,一定 |
不一定 |



(4)气密度(m总为气体总质量)

注意:恒容时,不用考虑系数
Ⅰ.恒温恒容密闭容器
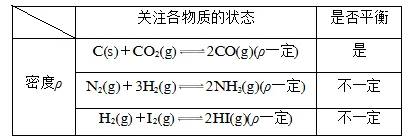

Ⅱ.恒温恒压密闭容器
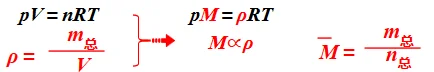
与 ρ成正比,故可通过来判断ρ是否为变量

【微点拨】理解平衡状态判定标志 (有正有逆符合比例;变量不变即平衡)
(1)全部是气体参加的非等体积反应,体系的压强、平均相对分子质量不再随时间而变化。
(2)对同一物质而言,断裂的化学键的物质的量与形成的化学键的物质的量相等。
(3)对于有色物质参加或生成的可逆反应,体系的颜色不再随时间而变化。
(4)绝热体系的温度不变,说明反应处于平衡状态。
(5)全部是气体的非等体积反应,恒压条件下,密度不再变化;对于有固体参与或生成的气体平衡体系,密度不再变化。
总之,要抓住变化的量不变可作平衡的标志;如果该物理量始终是一个定值,就不能作为判断是否达平衡的标志。
|
举例 |
|
状态 |
|
混合物体系中各成分的含量 |
各物质的物质的量或各物质的物质的量分数一定 |
平衡 |
|
各物质的质量或各物质的质量分数一定 |
平衡 |
|
|
各气体的体积或体积分数一定 |
平衡 |
|
|
总压强、总体积、总物质的量一定 |
不一定平衡 |
|
|
正、逆反应速率的关系 |
在单位时间内消耗了m mol A,同时生成m mol A, 即v正=v逆 |
平衡 |
|
在单位时间内消耗了n mol B,同时生成p mol C |
不一定平衡 |
|
|
vA∶vB∶vC∶vD=m∶n∶p∶q,v正不一定等于v逆 |
不一定平衡 |
|
|
在单位时间内生成了n mol B,同时消耗了q mol D |
不一定平衡 |
|
|
压强 |
m+n≠p+q时,总压强一定(其他条件一定) |
平衡 |
|
m+n=p+q时,总压强一定(其他条件一定) |
不一定平衡 |
|
|
混合气体的平均相对分子质量 |
|
平衡 |
|
|
不一定平衡 |
|
|
温度 |
任何化学反应都伴随着能量的变化,在其他条件不变的情况下,体系温度一定 |
平衡 |
|
密度 |
密度一定 |
不一定 平衡 |
|
颜色 |
含有有色物质的体系颜色不再变化 |
平衡 |
|
浓度商 |
Q=K |
平衡 |


